 A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta quinta-feira (8) o início de testes de anticorpos contra covid-19 desenvolvidos pela farmacêutica AstraZeneca.
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta quinta-feira (8) o início de testes de anticorpos contra covid-19 desenvolvidos pela farmacêutica AstraZeneca.
O AZD7442 é uma combinação de dois tipos de anticorpos de longa ação sintetizados a partir do plasma convalescente de pessoas recuperadas da covid-19.
Em outros países, os testes são conduzidos tanto para saber a capacidade de prevenir a covid-19 (profilaxia) como para tratar quem já foi exposto ou está doente.
Segundo a AstraZeneca, esses anticorpos foram projetados para reduzir o risco de resistência desenvolvida pelo SARS-CoV-2.
Um ensaio avalia a segurança e eficácia do AZD7442 para prevenir a infecção por até 12 meses, em aproximadamente 5.000 participantes.
O segundo estudo envolve a profilaxia pós-exposição e o tratamento preventivo em aproximadamente 1.100 participantes, anunciou a empresa em outubro do ano passado.
"Uma combinação LAAB (anticorpos de longa duração, na sigla em inglês) pode ser complementar às vacinas como agente profilático, por exemplo, para pessoas para as quais uma vacina pode não ser apropriada ou para fornecer proteção adicional para populações de alto risco. Também pode ser usado para tratar pessoas infectadas", acrescenta a companhia.
Embora a autorização da Anvisa tenha saído no Diário Oficial de hoje, ainda não há detalhes de como os estudos serão conduzidos no Brasil.
R7
Foto: Divulgação/NIAID-RML















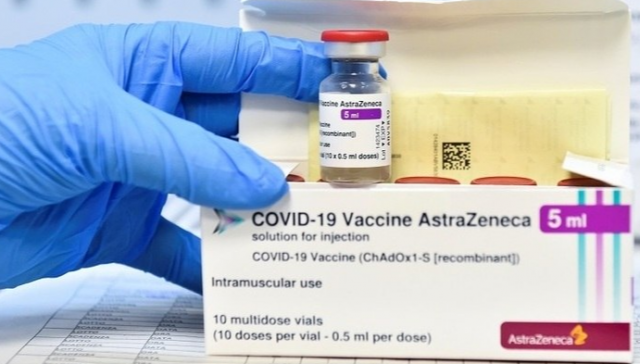 A vacina anticovid criada pela AstraZeneca/Oxford ainda apresenta "amplamente" mais benefícios do que riscos, anunciou a OMS (Organização Mundial da Saúde) nesta terça-feira (6).
A vacina anticovid criada pela AstraZeneca/Oxford ainda apresenta "amplamente" mais benefícios do que riscos, anunciou a OMS (Organização Mundial da Saúde) nesta terça-feira (6). A chegada da temporada da gripe é um fator complicador para a campanha nacional de enfrentamento à Covid-19. Além de gerar situações de co-infecções - por mais de um vírus, a própria prevenção às gripes comuns, por meio da vacinação, compromete a capacidade brasileira de produção de imunizantes contra a covid-19.
A chegada da temporada da gripe é um fator complicador para a campanha nacional de enfrentamento à Covid-19. Além de gerar situações de co-infecções - por mais de um vírus, a própria prevenção às gripes comuns, por meio da vacinação, compromete a capacidade brasileira de produção de imunizantes contra a covid-19.