 Pousou na tarde desta segunda-feira, 18, o avião da Força Aérea Brasileira (FAB) com as primeiras 61.160 mil doses da vacina Coronavac, por volta das 15:00h, no Aeroporto Petrônio Portella, localizado na zona norte de Teresina.
Pousou na tarde desta segunda-feira, 18, o avião da Força Aérea Brasileira (FAB) com as primeiras 61.160 mil doses da vacina Coronavac, por volta das 15:00h, no Aeroporto Petrônio Portella, localizado na zona norte de Teresina.
A aeronave decolou do Aeroporto de Guarulhos, em São Paulo, por volta das 10h30 de hoje, logo após o ministro da Saúde, Eduardo Pazuello autorizar o início da vacinação já nesta segunda em todo o país.
O Piauí inicia ainda hoje a vacinação com a Coronavac. Cinco profissionais da saúde que trabalham nas unidades hospitalares que compõem a Rede Estadual serão os primeiros que serão vacinados. A cerimônia será realizada no pátio da Sesapi, às 17 horas.
Os profissionais atuam nos Instituto de Doenças Tropicais Natan Portella; Hospital Getúlio Vargas; Hospital da Polícia Militar; Hospital Infantil Lucídio Portella e Maternidade Dona Evangelina Rosa.
Uso emergencial aprovado
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, na tarde deste domingo (17), por unanimidade, o uso emergencial da Coronavac e da vacina de Oxford/AstraZeneca.
A reunião extraordinária que teve início às 10h10 e terminou às 15h20, contou com a votação de cinco diretores: Meiruze Sousa Freitas (relatora); Antonio Barra Torres (diretor-presidente); Cristiane Rose Jourdan Gomes (médica e bacharel em direito); Romison Rodrigues Mota - substituto (servidor da Anvisa); e Alex Machado Campos (advogado).
A diretora da Anvisa e relatora, Meiruze Freitas, votou pela aprovação e destacou que é preciso que o Instituto Butantan assine um termo de compromisso para apresentar dados de imunogenicidade da vacina até 28 de fevereiro (os relatórios sobre o tema foram considerados insuficientes). O termo assinado foi publicado em Diário Oficial da União.
Já a decisão sobre a vacina de Oxford vale apenas para o uso das 2 milhões de doses que o governo ainda tenta importar da Índia.
GP1














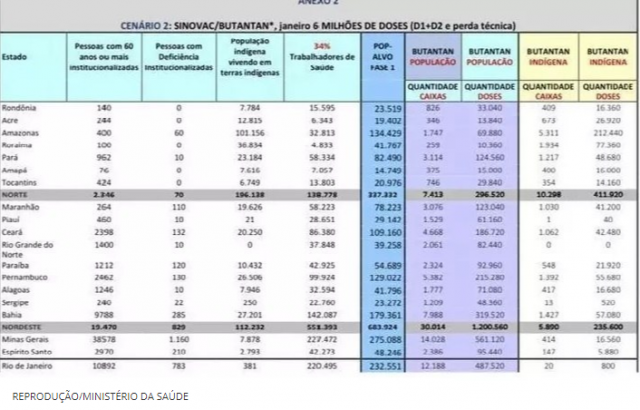
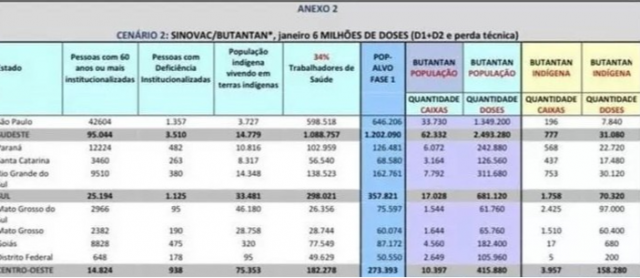
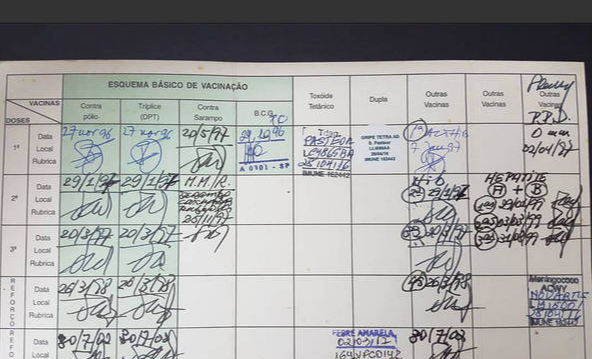 A vacinação nacional contra a covid-19, prevista para ter início na quarta-feira (20), conforme anunciado pelo ministro da Saúde Eduardo Pazuello durante reunião com prefeitos na quinta-feira (14), contará com carteira digital, para registro da dose da vacina, e possibilidade de ser imunizado apenas apresentando o CPF.
A vacinação nacional contra a covid-19, prevista para ter início na quarta-feira (20), conforme anunciado pelo ministro da Saúde Eduardo Pazuello durante reunião com prefeitos na quinta-feira (14), contará com carteira digital, para registro da dose da vacina, e possibilidade de ser imunizado apenas apresentando o CPF.